ここまで循環とは何かの話をメインにやってきました。
前回は輸液反応性についてを先にやってしまいました。少し脇道に逸れますが、輸液の話をしようと思います。輸液そのものについての話を学ぶことがあまりないので、この辺を横着しがちです。
・「1:3:8」が、、、血管内、間質、細胞外液、、
この辺は国家試験でよく言われることで、よく皆さんご存知だと思います。
正直、この辺も勿論知識として必要ですが、正しい輸液、ひいてはボリューム管理についてはそんなことよりも大事な生理学があります。浸透圧とか色々な話がでてきて、生理学が嫌いな人には拒絶反応が出そうですが、なるべく基本的なところをかいつまんで説明しようと思います。
【1】OsmolalityとTonicity
(1)晶質浸透圧と膠質浸透圧
晶質浸透圧→電解質やブドウ糖
膠質浸透圧→Albなどタンパク質
まずこの辺の指導をするときに、何はなくとも「晶質と膠質の違いはわかりますか?」から始めます。
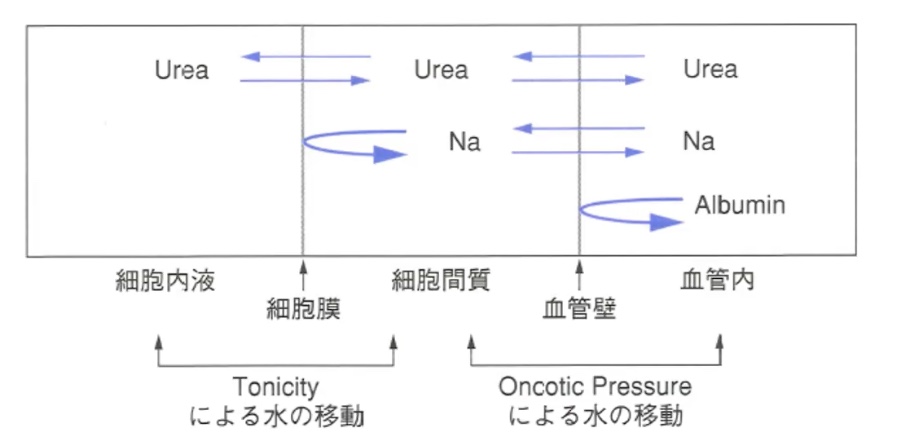
(1)晶質浸透圧→「細胞外液(間質+血管)に水を引き付ける」
細胞膜を介して細胞内外を行き来する(特に細胞内液と組織間液の間で)これによって圧(分子量)変化をもたらすことで水の出入りを生む
(2)膠質浸透圧→「血管内に水をひきつける」
基本的にはアルブミン。
これらは血管内からでていくことはまずない。
毛細血管の中に存在し、膠質として水を血管内に引き付ける。
対して晶質であるその他の物質は毛細血管を自由に行き来することができるので、それと水の移動で静水圧を生む。
静水圧と膠質浸透圧の均等が概ねとれたところに落ち着く。
晶質との違いは
①晶質と違い自由に出入りできない
②分子量が莫大にでかいため、分子数(mOsmとして)はしょぼいので、それ程
浸透圧差を産まない
③「晶質は細胞内から間質に」「膠質は間質から血管内に」水分を惹きつける
※effective osmoleとnon-effective osmole
少しレベルを上げます。
上図において、細胞膜を透過するか否か(Tonicityに影響するか)がポイント。
その上で、浸透圧物質の中でも、「細胞膜を透過せずにTonicity(細胞外に水を引き付ける力)を形成する物質」をeffective osmole、
non-effective osmoleは勝手に透過してしまうもの
と定義します。
つまり、血漿浸透圧を計算するときには

上記になるが、Tonicityの計算をするときには、

non-effective osmoleを差し引いて考えなくてはならない。
つまり、上記の式において血管内外の棲み分けを考える際には、NaとGluを基本的には考えればよい。
しかし実臨床上はほとんどNaのみを考慮する。
①この数値の計数の差
②Gluは血管内に入って比較的速やかに代謝される
そのため、5%GluはTonicityを持ちそうであるが、血管内に入ってすぐにfree water扱いとなるのである。
※蒸留水を投与してはいけない理由、5%Gluがよい理由。
蒸留水は浸透圧0であり、浸透圧差の問題で、赤血球が膨張して破壊、溶血しまうので。
これはよくご存知だろう。
5%Gluは(一応)浸透圧を持つので、上記はおこらないが、すぐにfree waterになる。
水を入れるイメージで5%Gluを入れるのである。
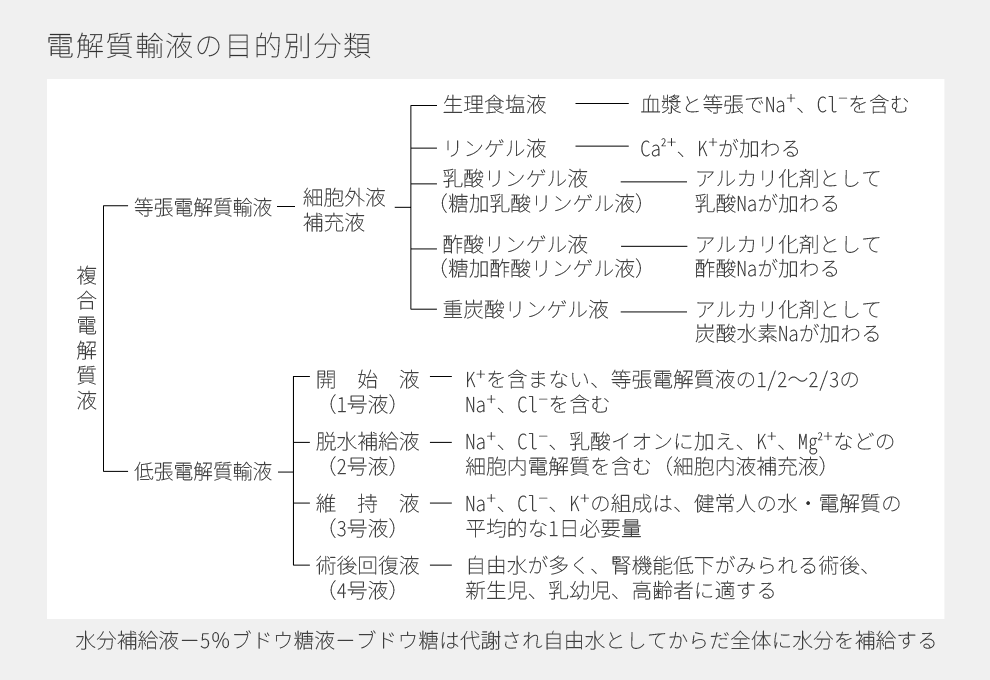
cf. 大塚製薬Hp
上記を見ると、
①等張電解質輸液
②低張電解質輸液
に大別される。
等張輸液は輸液のOsmolalityが(概ね)血漿内と同等であることを指す。
それの代表格が生理食塩水であり、他等張輸液も浸透圧比(生理食塩水の浸透圧を1としたときの比率)は1であるはずである。
では、低張輸液はどうか?
先述した通り、浸透圧比が低ければ血管内に入ってから、溶血をおこしてしまいそうなものである。
低張輸液は等張輸液と比較して「電解質の占める浸透圧が足りていない」、それを、蒸留水ではなく、5%Gluを投与するように、Gluを足すことで、浸透圧比を1にする。
Osmolality, Tonicityがごっちゃになってしまっているのが難儀であるが、輸液の浸透圧比は1に設定されていることがわかる。
これはあくまで晶質浸透圧の話。
※(Adv)膠質浸透圧(以下COP:colloid osmotic pressure)のはなし。
実際に測定できるようになったため、TP、Albで近似すると下記になる。
①COP = 1.8 × TP × Abs + 5.5
②COP = 2.1 × TP + 0.16 × TP2 + 0.009 × TP3
(TP:total protain, Abx:280nmにおいての血清吸光度)
上記のように近似されるとされる。
実臨床においてAlbに引っ張られがちだが、TP全体として考えなくてはいけないのである。
【2】実際に輸液をしてみると、、、、
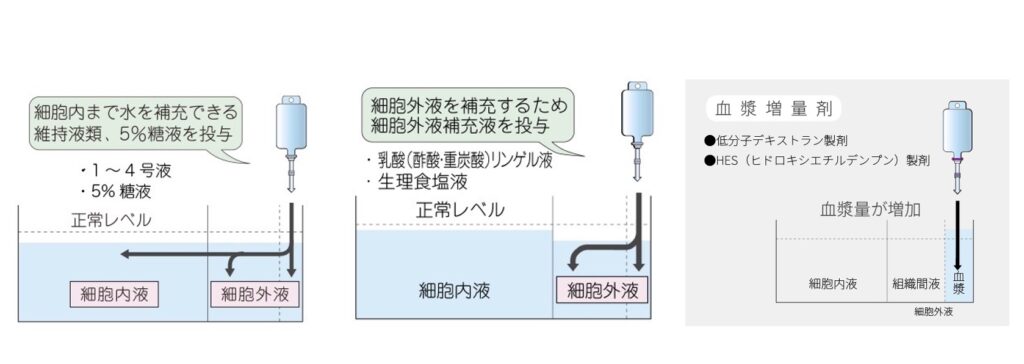
上図のようになる。
①低張輸液
5%Gluであれば完全にfree waterとして、たとえば1号液なら[Na+]=90程度の分、外液にも分布する。
②等張輸液
理論上は十分はTonicityをもって、細胞膜を透過せずに外液内で分布する。
③血漿増量剤
AlbやHES製剤など。血漿のみに分布して、「膠質浸透圧」として水を血漿内に引っ張る。
因みにHESやデキストランはGluの超重合体であり、分子量が5桁にも至り「膠質浸透圧」として働く。
※高Cl性アシドーシス?
血管内脱水の際に生理食塩水を使用すると「高Cl性アシドーシス」が起こるという。
血管内に生理食塩水を入れ続けると、血漿の電解質が限りなくNa, Clの値が154に近づいていく。もちろん細胞内への移動などもあるが、限りなく近づいているのである。
すると、陰イオンがClで満たされていき、陰イオンとしてのHCO3の居場所がなくなっていく(細胞内への移動、もしくは代謝されたりする)。
すると血管内のHCO3は少なくなっていき、代謝性のアシドーシスになる。
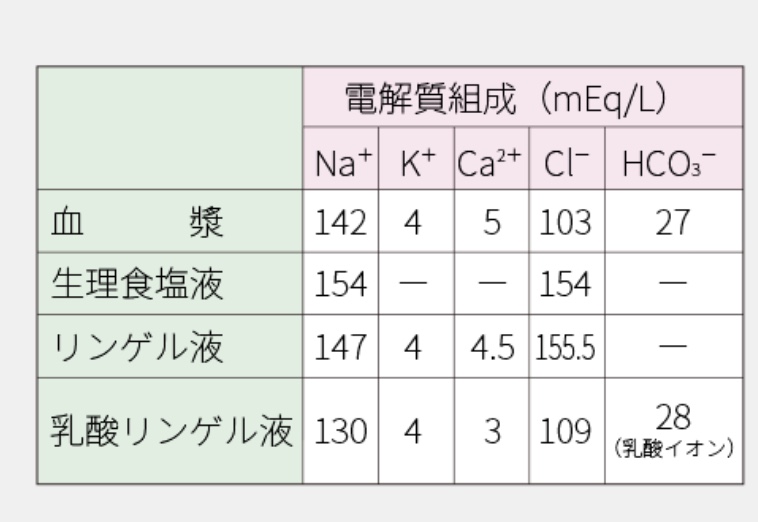
※乳酸リンゲルや酢酸リンゲルにすると良い理由。
ソルラクト、ソルアセトなどである。
これらはClが少ない代わりに、陰イオンとしての乳酸イオンや酢酸イオンが使われる。これらは乳酸や酢酸が代謝されることによってHCO3に変換されるので、概ね血漿成分に近づいた生理的な組成になってくれるのである。
Q, 乳酸リンゲルと酢酸リンゲルはどっちを使えばいいの?
A, 本当にどっちでもいい。
内容する電解質も微差である。
代謝経路が異なり、乳酸が肝臓メイン、酢酸が腎臓メインで代謝される。(乳酸は本来イメージ通り骨格筋で多く酸化されていくがここでは割愛する)
なので、厳密に言えば腎不全があれば乳酸リンゲルであり、肝不全があれば酢酸リンゲルがよさそうである。
リンゲル液同士の比較のRCTなどもあるが差異なく気にせずつかっていい。cf.HEMACETAT
生理食塩水と比較して転帰がいい。cf. SALT ED
Q, 手術室で上記の輸液を使っているのを見たことないが?
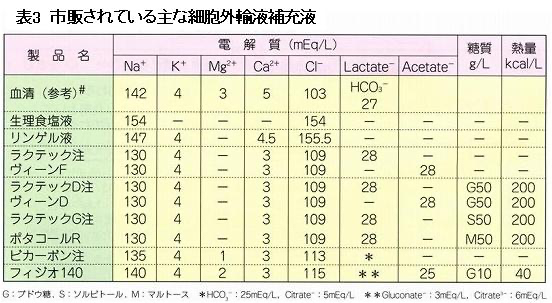
手術室で一番見るのがビカネイト/ビカーボンやフィジオであり、2番目がボルベンだろうか。
まず、ビカネイトから。
これは重炭酸リンゲルである。
乳酸、酢酸の部分に直接重炭酸が入っている。
もちろんこれは非常に生理的であり、切迫する状況であればこちらの方がいいに決まっている。しかしながら先述した通り、少し時間が経てば概ね乳酸リンゲルや酢酸リンゲルも同じように振る舞うのでそれほど問題はない。
次にフィジオ。
フィジオは酢酸が緩衝材となっているものの、
①Naが近い
②Mgが含有されている
これらから血漿と近く生理的である。
続いて、ボルベン(分子量13万)の話をする。
※血症増量剤、特にボルベンについて
これは【2】-③の血漿増量剤である。
ヘスパンダー(分子量7万)もある。
これらはHES(ヒドロキシエチルデンプン)製剤である。あまりに分子量が大きいため、血管外に出ていくことが少ない。
大きければ大きい方がいいわけではなく、以前は海外では分子量45万のHES製剤が作られたことがあるが、代謝されることがなく、腎不全への影響が出てきたこと、凝固因子への異常をきたしたため今では使用されることはない。
つまり大きければ大きいほどいいというわけでもなさそうである。
一般的にボルベンの方を使うことが多いのでこちらを説明する。
①生理食塩水が基材
②出血の有無に関わらず使用可能
③血管内にほとんど100%残留する
③50ml/kg/dayまで使用可能(ヘスは1Lまで)
※重症患者全員にアルブミン製剤やHES製剤をいかない理由。
(1)まず適応のはなし。
先述のメリットも含めて、ボルベンの方がへスパンダーに比べて適応が広い。
つづいて、Alb製剤。
幅広い適応があり、使うとよいのだが、HES製剤と比べて圧倒的高価であることがデメリットとして挙げられる。適応などについては「科学的根拠に基づいたアルブミン製剤の使用ガイドライン」がよくまとまっており一読されたい。
よく使うケースとして想定される
・Hypovolemic shock
・septic shock
についての記載を読むと、どちらも推奨されないとされる。
特にsepsisにおいては、Albではなく、晶質液を使用するように記載されている。
これはALBIOS studyなどのRCTにてAlb製剤による死亡率減少を認めず、晶質液と有意差がないことに起因する。
※アルブミン製剤について
①デメリット
Alb製剤は一般的な輸液のみと比較して、予後を改善しない。
それどころか、熱傷や低アルブミン血症の患者に対しては予後をかえって悪くする。
PMID:9677209
②メリット
・Alb製剤は投与することで抗炎症作用をもたらす。
cf. Critical care 2015;19:156
・Alb製剤は一般的な輸液のみと比較して、敗血症性ショックの患者に対して死亡率を下げる。PMID: 37762860
デメリットのRCTは1998、メリットのmetaは2023であるが、現時点でどちらが正しいかといいきるのは難しい。
実際、中身もいいもの悪いものとされるものが分散されており、判断に苦慮する。
包括して考えると、sepsisはよさそう、熱傷は悪そう、である。
基本的にはアルブミンは先述の通り、「血管内」にすべて留まるはずである。
しかしながらそうはいかないのは、細胞間質に漏れ出る経過を辿るからである。
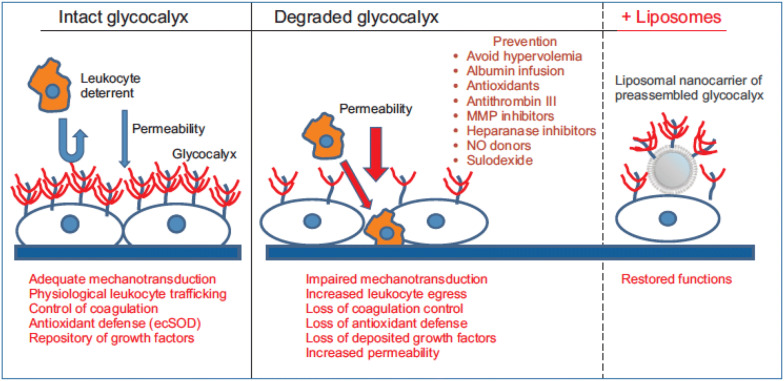
それはなぜか、下図のよる、間質との間にはGlycocalyxという線毛のようなものが存在している。
下図のintactつまり、健常なglycocalyxが保たれている時には、凝固のコントロールや、アルブミンが漏れ出るのを防ぐことができる。(左)
しかしながら、敗血症やその他の重症病態の患者ではそうはいかず、Degraded(中央)のglycocalyxとなる。Glycocalyxが剥げ落ちていき、細胞間接着が緩んでいく。
その結果、Alb含めた種々の蛋白質などが漏れ出てしまうのである。
そのため、Alb製剤などを用いていきたい重症病態では特に、これらの製剤が計算通りにうまく機能しないことを頭にいれておく必要がある。
(3)へスパンダー
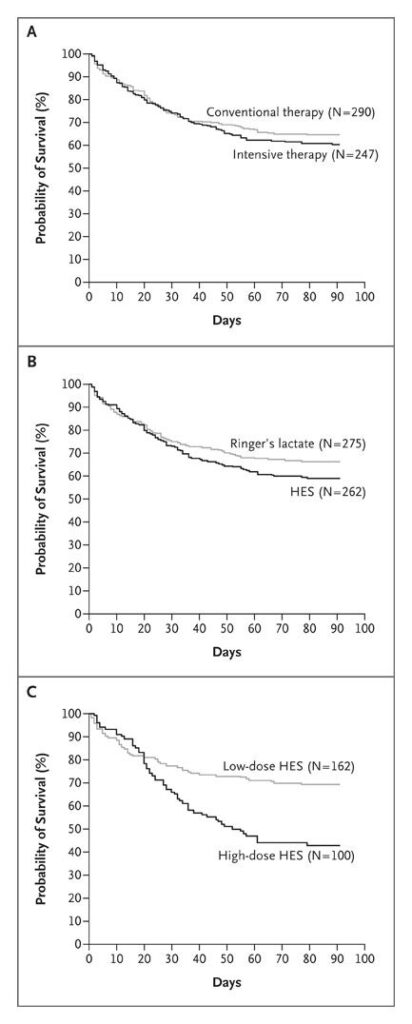
リンゲル液とHESで比較した場合、HES使用の方が死亡率が高いとされる。
また高容量は低容量と比較して死亡率が高いとされる。
これらがなぜ起こるかは下記の結果から推測される。
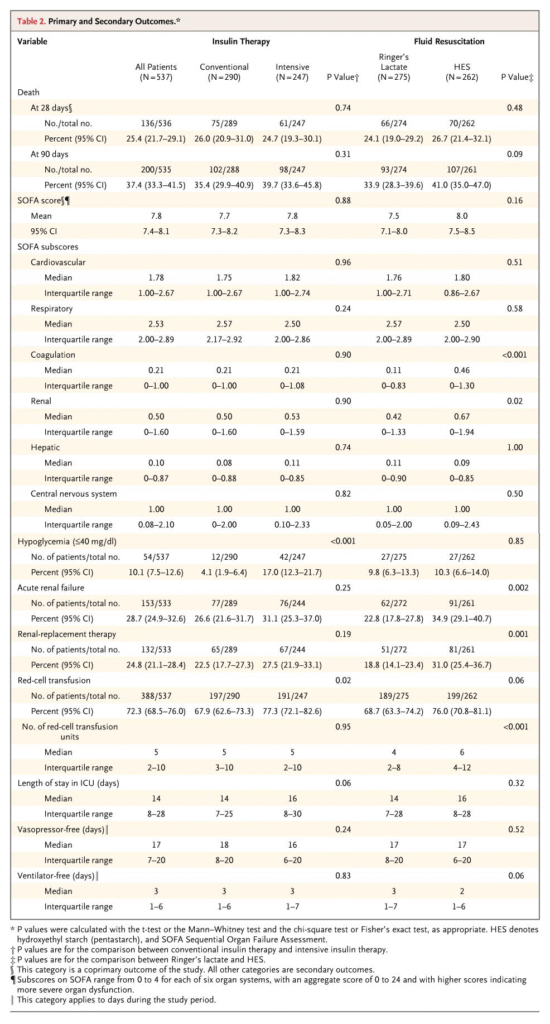
上記を見てみると、HES使用にて腎障害が起きやすくなるからであると考えられる。
HESなどの超高分子量の物質にて腎性のAKIが新規におこるためであると考える。
cf.N Engl J Med 2008;358:125-139